Характеристика Элементов Таблицы Менделеева
В соответствии с закономерностями для упомянутых характеристик, наиболее ярко выраженные металлы располагаются в начале . Характеристика элементов по положению в таблице Менделеева. Центр онлайн-обучения «Фоксфорд». Онлайн-школа с 3 по 11 класс. Периодическая таблица элементов является графическим выражением. Менделеева, но она уже.
Характеристика химического элемента на основании его положения в Периодической системе элементов Менделеева Д.И. Найдено документов - 4. Обычно характеристику химического элемента дают по следующему плану. Волосы Симс 3 здесь.
Характеристика Элементов Таблицы Менделеева 8 Класс
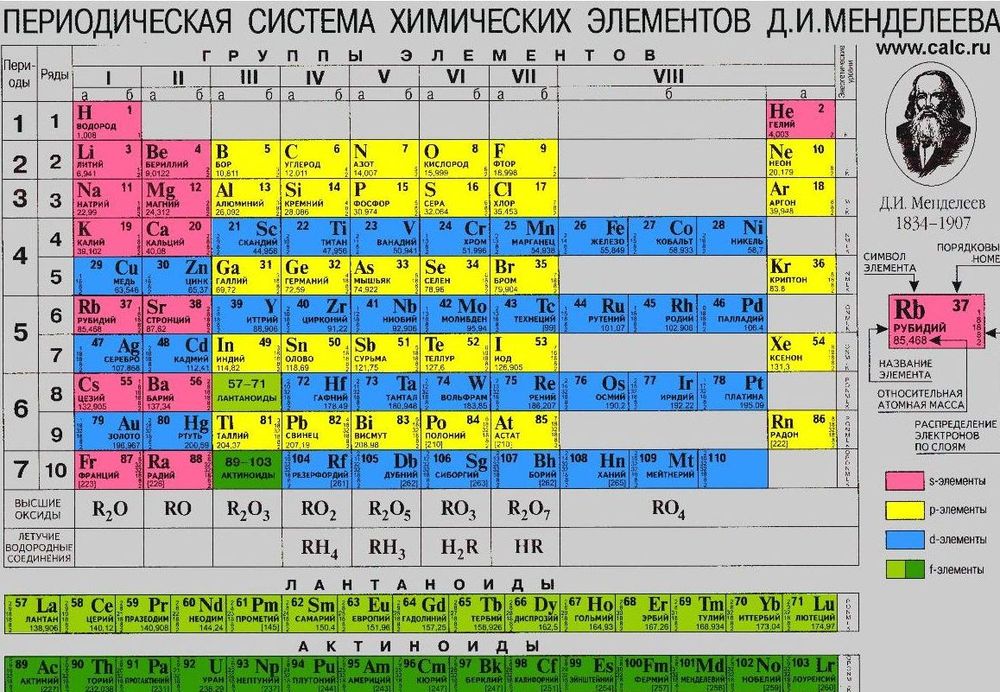
Периодическая система химических элементов — Википедия. Периодическая таблица химических элементов. Периоди. Система является графическим выражением периодического закона, установленного русским химиком Д. Менделеевым в 1. 86. Её первоначальный вариант был разработан Д. Менделеевым в 1. 86.
Всего предложено несколько сотен. В современном варианте системы предполагается сведение элементов в двумерную таблицу, в которой каждый столбец (группа) определяет основные физико- химические свойства, а строки представляют собой периоды, в определённой мере подобные друг другу. К середине XIX века были открыты 6.
В 1. 82. 9 году. Дёберейнер опубликовал найденный им «закон триад»: атомная масса многих элементов близка к среднему арифметическому двух других элементов, близких к исходному по химическим свойствам (стронций, кальций и барий; хлор, бром и иод и др.). Первую попытку расположить элементы в порядке возрастания атомных весов предпринял Александр Эмиль Шанкуртуа (1.

Обе указанные модели не привлекли внимания научной общественности. В 1. 86. 6 году свой вариант периодической системы предложил химик и музыкант Джон Александр Ньюлендс, модель которого («закон октав») внешне немного напоминала менделеевскую, но была скомпрометирована настойчивыми попытками автора найти в таблице мистическую музыкальную гармонию.
Полная Характеристика Элементов Таблицы Менделеева
В этом же десятилетии появились ещё несколько попыток систематизации химических элементов; ближе всего к окончательному варианту подошёл Юлиус Лотар Мейер (1. Однако главное отличие было в том, что за основу периодичности была взята валентность, которая не является единственной и постоянной для отдельно взятого элемента, в результате чего такая таблица не может претендовать на полноценное описание физики периодического закона. Менделеев опубликовал свою первую схему периодической таблицы в 1. Соотношение свойств с атомным весом элементов» (в журнале Русского химического общества); ещё ранее (февраль 1. Днём открытия периодического закона считается 1 марта (1.
Д. Менделеев закончил работу над «Опытом системы элементов, основанной на их атомном весе и химическом сходстве». И только в декабре выходит работа немецкого химика Мейера, который изменил своё решение в пользу мысли Д.
Менделеева и в зарубежной литературе считается либо «одним из первооткрывателей», либо «независимо от Менделеева опубликовавшим этот периодический закон». По легенде, мысль о системе химических элементов пришла к Менделееву во сне, однако известно, что однажды на вопрос, как он открыл периодическую систему, учёный ответил: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг. Итогом работы стал отправленный в 1.
России и других стран первый вариант системы («Опыт системы элементов, основанной на их атомном весе и химическом сходстве»), в котором элементы были расставлены по девятнадцати горизонтальным рядам (рядам сходных элементов, ставших прообразами групп современной системы) и по шести вертикальным столбцам (прообразам будущих периодов). В 1. 87. 0 году Менделеев в «Основах химии» публикует второй вариант системы («Естественную систему элементов»), имеющий более привычный нам вид: горизонтальные столбцы элементов- аналогов превратились в восемь вертикально расположенных групп; шесть вертикальных столбцов первого варианта превратились в периоды, начинавшиеся щелочным металлом и заканчивающиеся галогеном.
Каждый период был разбит на два ряда; элементы разных вошедших в группу рядов образовали подгруппы. После определённого количества разных по свойствам элементов, расположенных по возрастанию атомного веса, свойства начинают повторяться. Например, натрий похож на калий, фтор похож на хлор, а золото похоже на серебро и медь. Разумеется, свойства не повторяются в точности, к ним добавляются и изменения. Отличием работы Менделеева от работ его предшественников было то, что основ для классификации элементов у Менделеева была не одна, а две — атомная масса и химическое сходство.
Для того, чтобы периодичность полностью соблюдалась, Менделеевым были предприняты очень смелые шаги: он исправил атомные массы некоторых элементов (например, бериллия, индия, урана, тория, церия, титана, иттрия), несколько элементов разместил в своей системе вопреки принятым в то время представлениям об их сходстве с другими (например, таллий, считавшийся щелочным металлом, он поместил в третью группу согласно его фактической максимальной валентности), оставил в таблице пустые клетки, где должны были разместиться пока не открытые элементы. В 1. 87. 1 году на основе этих работ Менделеев сформулировал Периодический закон, форма которого со временем была несколько усовершенствована. Научная достоверность Периодического закона получила подтверждение очень скоро: в 1. Менделеев, пользуясь периодической системой, предсказал не только возможность их существования, но и с поразительной точностью описал целый ряд физических и химических свойств. В начале XX века с открытием строения атома было установлено, что периодичность изменения свойств элементов определяется не атомным весом, а зарядом ядра, равным атомному номеру и числу электронов, распределение которых по электронным оболочкаматома элемента определяет его химические свойства.
Дальнейшее развитие периодической системы связано с заполнением пустых клеток таблицы, в которые помещались всё новые и новые элементы: благородные газы, природные и искусственно полученные радиоактивные элементы. В 2. 01. 0 году, с синтезом 1. Менделеева остаётся одной из важнейших в современной теоретической химии. Наименование было предложено коллективами Объединенного института ядерных исследований и Ливерморской национальной лаборатории. В «сверхдлинном» варианте каждый период занимает ровно одну строчку.
В «длинном» варианте лантаноиды и актиноиды вынесены из общей таблицы, делая её более компактной. В «короткой» форме записи, в дополнение к этому, четвёртый и последующие периоды занимают по 2 строчки; символы элементов главных и побочных подгрупп выравниваются относительно разных краёв клеток. Водород иногда помещают в 7- ю («короткая» форма) или 1. Несмотря на рекомендацию использовать длинную форму, короткая форма продолжает приводиться в большом числе российских справочников и пособий и после этого времени. Из современной иностранной литературы короткая форма исключена полностью, вместо неё используется длинная форма.
Характеристика химического элемента по его положению в Периодической системе — Науколандия. Факт того, что свойства химических элементов периодически изменяются было известно до открытия Периодического закона Д. Менделеевым. Заслуга Менделеева в том, что он открыл закон природы, лежащий в основе этой периодичности. Именно используя этот закон, была составлена периодическая таблица химических элементов.
Во времена Менделеева были открыты еще далеко не все химические элементы, поэтому составление таблицы было достаточно сложным делом. Менделеев предположил существование некоторых элементов, что вскоре было подтверждено их открытием. Характеризуют химический элемент по следующему плану. Определяют период, группу и подгруппу химического элемента в Периодической таблице, его порядковый номер и относительную атомную массу. Например, Si (кремний) находится в 3 периоде, IV группе, главной подгруппе (A), его порядковый номер 1. Определяют является химический элемент металлом или нет. Металлические свойства убывают слева направо и возрастают сверху вниз.
Кремний расположен ниже углерода (который неметалл) и выше галлия (который уже проявляет металлические свойства). Если смотреть по периоду то до кремния находится алюминий (металл), а после него — фосфор (неметалл). Таким образом, сделать вывод о том, чем является кремний достаточно сложно. Это надо знать. Кремний — это неметалл. Определяют максимальную валентность элемента и составляют формулу его высшего оксида. Так как кремний находится в IV группе, то его максимальная валентность равна IV, а высший оксид — Si. O2. Данному оксиду соответствует кремниевая кислота, следовательно, он кислотный.
Если элемент неметалл, то для него указывают формулу водородного соединения. Гидрид кремния — Si.